Glosario
O | P | Q | R | S | T | U | V | W | X | Y | Z
-
P
- Páncreas (Cáncer)
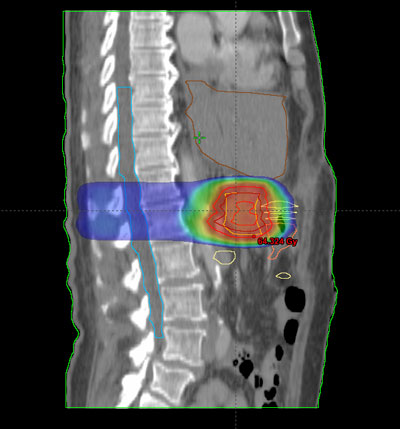
Cuando las células tumorales están ubicadas en el páncreas hablamos de cáncer de páncreas.
Cáncer de páncreas exocrino:
Las formas más habituales de cáncer de páncreas exocrino son los adenocarcinomas. Constituyen la gran mayoría de los tumores de este órgano (más del 95 %). Afectan a las células encargadas de la elaboración de los jugos digestivos y se localizan más frecuentemente en la zona de la cabeza pancreática.
Son mucho menos frecuentes los tumores del cuerpo y aún más infrecuentes los situados en la cola pancreática.
Son muy raros otros tipos de cáncer como linfomas y sarcomas.
Cáncer de páncreas endocrino:
Se consideran aparte los cánceres que afectan a las células en las que tiene lugar la síntesis de sustancias hormonales. Estos son mucho más raros (insulinomas, glucagonomas...) Poseen un curso diferente al resto de tumores pancreáticos, tanto en los síntomas como en el diagnóstico y tratamiento.
Para determinar el tratamiento más adecuado para cada caso de cáncer de páncreas, es importante clasificar el tumor y determinar en qué fase se encuentra.El sistema que con mayor frecuencia se emplea para su clasificación es el TNM. Estas siglas hacen referencia a tres aspectos del cáncer: la T se refiere al tamaño del tumor, la N a la afectación de los ganglios linfáticos y la M a la afectación o no de otros órganos.
En función de estos aspectos, la enfermedad se agrupa en las siguientes etapas o estadios:- Estadio I: el tumor afecta sólo al páncreas.
- Estadio II: el tumor afecta al duodeno o a la vesícula biliar, pero no a ganglios linfáticos.
- Estadio III: en esta etapa el tumor afecta alos ganglios linfáticos independientemente de su tamaño.
- Estadio IV: el cáncer se ha diseminado afectando a otros órganos como estómago, colon, hígado o más infrecuentemente pulmón.
Elección del tratamiento
Una vez confirmado el diagnóstico de cáncer de páncreas y tras realizar las pruebas necesarias para conocer en qué fase está la enfermedad, se debe determinar cuál es el tratamiento más adecuado.El especialista recomendará y explicará las posibilidades de tratamiento más adecuadas a su caso, para que una vez que haya recibido la suficiente información pueda, junto con su médico, tomar una decisión.
El plan de tratamiento del cáncer de páncreas es multidisciplinario y se basa en una serie de normas y pautas (protocolo), establecidas por cada hospital basándose en la experiencia clínica.
Estos protocolos, recogen las indicaciones o limitaciones de tratamiento en función de una serie de factores:- Fase en la que se encuentra la enfermedad (TNM).
- El tipo de célula que forma el tumor.
- Edad del paciente.
Probablemente, el médico también tendrá en cuenta, si además del cáncer de páncreas, existen otras enfermedades importantes que puedan dificultar la realización de algún tratamiento específico.
Por tanto el tratamiento propuesto por el especialista no va a ser el mismo en todos los pacientes.
Los tratamientos más frecuentemente empleados en el cáncer pancreático son la cirugía, la radioterapia y la quimioterapia. Independientemente de estos, el médico se encargará de tratar específicamente aquellos síntomas que presenta el enfermo.
Cáncer del páncreas en estadio I y estadio II
El tratamiento del cáncer de páncreas en el estadio I y en estadio II puede incluir los siguientes procedimientos:
- Cirugía sola.
- Cirugía con quimioterapia y radioterapia.
Cáncer del páncreas en estadio III
El tratamiento del cáncer del páncreas en el estadio III puede incluir los siguientes procedimientos:
- Cirugía paliativa o colocación de cánulas para evitar las áreas bloqueadas en los conductos o en el intestino delgado.
- Quimioterapia con gemcitabina.
Cáncer del páncreas en estadio IV
El tratamiento del cáncer del páncreas en el estadio IV puede incluir los siguientes procedimientos:
- Quimioterapia con gemcitabina, con erlotinib o sin este.
- Tratamientos paliativos para el dolor, como bloqueo de los nervios y otros cuidados médicos de apoyo.
- Cirugía paliativa o colocación de cánula para evitar las áreas bloqueadas en los conductos o en el intestino delgado.
Opciones de tratamiento para el cáncer del páncreas recidivante
El tratamiento del cáncer de páncreas recidivante puede incluir los siguientes procedimientos:
- Quimioterapia.
- Cirugía paliativa o colocación de una cánula para evitar áreas bloqueadas en conductos o en el intestino delgado.
- Radioterapia paliativa.
- Otras medidas médicas paliativas para reducir los síntomas, como el bloqueo de nervios para aliviar el dolor.
Radioterapia
La radioterapia es el empleo de radiaciones ionizantes para el tratamiento, local o locorregional, de determinados tumores que emplea rayos X con altas dosis de irradiación.
Su objetivo es destruir las células tumorales causando el menor daño posible a los tejidos sanos que rodean dicho tumor.
En el cáncer de páncreas, la radioterapia no se emplea como tratamiento exclusivo con intención curativa, ya que las dosis necesarias para destruir el tumor serían elevadas y los efectos secundarios muy serios.
Cirugía
La cirugía es el tratamiento fundamental en aquellos tumores de páncreas operables, es decir que están limitados al mismo. En ocasiones, es necesario complementarla con otros tratamientos.
La cirugía del páncreas, en cualquiera de sus modalidades, es una intervención compleja. En todos los casos es preciso que el paciente permanezca ingresado en el hospital durante un tiempo que puede variar de un enfermo a otro, pero por lo general suele durar varias semanas. Asimismo, se requiere administrar una anestesia, que siempre será de tipo general.
El tipo de cirugía que se puede aplicar en este tipo de tumor, varía en función de la localización y de la extensión de la enfermedad a ganglios y/o órganos vecinos.
Las técnicas quirúrgicas más ampliamente empleadas son:
- Pancreatoduodenectomía o cirugía de Whipple: es la técnica más empleada para tratar el cáncer de páncreas. En general consiste en la extracción de la cabeza del páncreas. Para ello es preciso extirpar el duodeno (primera porción del intestino delgado), la vesícula biliar y el conducto secretor. En este tipo de operación se deja parte del páncreas para que pueda seguir funcionando, por lo que se conecta este al intestino delgado.
- También es posible en ocasiones que la zona extirpada sea sólo la región de la cola (pancreatectomía distal).
Con este tipo de cirugía es necesario administrar insulina al paciente para controlar los niveles de azúcar en sangre.
En ocasiones, la cirugía puede emplearse como tratamiento paliativo. Si el tumor está diseminado pero provoca una obstrucción de las vías biliares, lo indicado puede ser realizar un bypass. Consiste en la colocación de un tubo que rodee la zona de obstrucción, de tal forma que los jugos pancreáticos y la bilis pasen al intestino delgado sin pasar por la zona del tumor.
Cuando por determinadas circunstancias no sea posible llevar a cabo una cirugía, se puede colocar un pequeño tubo metálico o de plástico en la zona de la obstrucción (STENT) para que se abra el conducto y permita el paso de los jugos.
Generalmente estas 2 últimas técnicas mejoran los síntomas del enfermo e incrementan su calidad de vida.Quimioterapia
En el cáncer de páncreas la quimioterapia se puede emplear en las fases iniciales de la enfermedad tras la cirugía, generalmente asociada a la radioterapia (quimioterapia adyuvante).
En ocasiones la quimioterapia se administra antes de la cirugía (quimioterapia neoadyuvante) para reducir el tamaño tumoral y facilitar así su extirpación.
Cuando la enfermedad está más avanzada o el estado del paciente no permite aplicar cirugía, el tratamiento indicado para estos casos es la administración de quimioterapia pudiéndose asociar o no a la radioterapia. En estos casos, se emplea como tratamiento paliativo y su objetivo fundamental es disminuir los síntomas derivados del tumor y mejorar la calidad de vida del paciente.
Radioterapia
La radioterapia es el empleo de radiaciones ionizantes para el tratamiento, local o locorregional, de determinados tumores que emplea rayos X con altas dosis de irradiación.
Su objetivo es destruir las células tumorales causando el menor daño posible a los tejidos sanos que rodean dicho tumor.
En el cáncer de páncreas, la radioterapia no se emplea como tratamiento exclusivo con intención curativa, ya que las dosis necesarias para destruir el tumor serían elevadas y los efectos secundarios muy serios.
La radioterapia es útil en algunos casos en los que el tumor se ha diseminado a otros órganos y pudiera estar causando algún síntoma que disminuya la calidad de vida (radioterapia paliativa). Con dosis bajas de radiación se pueden mejorar dichos síntomas y aumentar el bienestar del paciente.
Asimismo, se puede emplear asociada a la quimioterapia tras la cirugía para eliminar las células que no se han podido extirpar. En este caso la dosis de radiación tampoco debe alcanzar dosis que pudieran lesionar los órganos más sensibles próximos al tumor.Planificación del tratamiento con RT:
Antes de empezar con el tratamiento propiamente dicho, es preciso realizar una planificación o simulación del mismo. Su finalidad es determinar una serie de parámetros que variarán dependiendo del tipo, de la localización y de la extensión del tumor, así como de las características anatómicas de cada enfermo.
Durante todo el tratamiento, el paciente ha de permanecer inmóvil y mantener la misma postura. Es frecuente, que próximo a la zona del tumor se encuentren determinadas estructuras importantes como el estomago, el hígado, riñones, medula espinal, entre otros. Para administrar la radiación con una precisión elevada y evitar que los tejidos sanos que rodean al tumor reciban más dosis de la tolerada, se utilizan sistemas de inmovilización muy precisos para que permitan la administración de la radiación con gran exactitud.
Habitualmente, para realizar el cálculo de la dosis que va a recibir tanto el tumor como los tejidos sanos de alrededor del mismo, es necesario realizar una tomografía de localización, cuyas imágenes se introducen en la computadora, donde se determina el volumen de tratamiento.
Antes de la realización de la tomografía se determina el sistema de inmovilización más adecuado para cada paciente según la técnica que se vaya a aplicar.
Una vez realizada la planificación, estos sistemas de fijación permiten su reproducción diaria en la sala de tratamiento.
¿Dónde se realiza el tratamiento con radioterapia?
Las habitaciones donde se realizan los tratamientos de radioterapia externa se llaman salas de radioterapia o búnkeres. Estas habitaciones poseen paredes de hormigón con un gran espesor que proporcionan un aislamiento perfecto impidiendo que la radiación salga fuera de ellas.
Mientras dura la sesión de tratamiento el paciente estará solo en el interior de la sala, pero vigilado por el personal especializado a través de un circuito de televisión y un interfono.
¿Por qué es necesario acudir todos los días?
Si se administrara toda la dosis de radiación en una única sesión se producirían daños muy serios en los tejidos. Para minimizar estos efectos secundarios, la dosis total de radiación se fracciona, repartiéndose en un número determinado de sesiones y días.
El fraccionamiento estándar consiste en administrar una sesión al día durante cinco días a la semana descansando dos, generalmente sábados y domingos. Para su administración no es necesario estar ingresado, puede acudir al hospital para el tratamiento y una vez finalizado volver a su casa.
¿Cuánto dura el tratamiento?
El tratamiento de radioterapia suele durar entre dos y siete semanas, dependiendo de la dosis que se administre y del número total de sesiones.
Diariamente, cada sesión dura sólo unos minutos (quince aproximadamente). El tiempo real de irradiación dura unos segundos.
Una vez finalizado el tratamiento diario, puede estar en contacto con otras personas, ya que no emite ningún tipo de radiactividad. Sus relaciones sociales, laborales y familiares no tienen por qué verse afectadas mientras dure el tratamiento.
Efectos secundarios:
La radioterapia, al mismo tiempo que elimina células enfermas, puede afectar a los tejidos sanos cercanos al área de tratamiento y como consecuencia aparecen efectos secundarios en la zona que ha recibido el tratamiento.
Estos efectos son difíciles de prever con exactitud, ya que dependen de múltiples factores como la zona del organismo donde se realiza el tratamiento, la dosis, el fraccionamiento y la susceptibilidad individual de cada persona. En algunos casos se producen efectos mínimos, mientras que en otros son más serios y es necesario administrar tratamiento médico para su control..
- Próstata (Cáncer)
Cáncer que se forma en los tejidos de la próstata (una glándula del aparato reproductor masculino que se encuentra debajo de la vejiga y adelante del recto). El cáncer de próstata se presenta, por lo general, en hombres de edad avanzada.
En el 95 % de los casos, el cáncer de próstata es un adenocarcinoma. Otros tipos menos frecuentes, por los que no se trata de ellos en estos apartados son el carcinoma de células transicionales (semejante al de la vejiga), el leiomiosarcoma, fibrosarcoma o linfoma.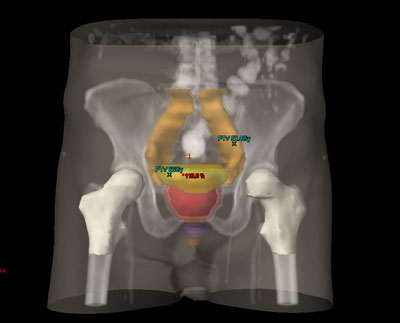
Para poder determinar el tratamiento más adecuado para el cáncer de próstata, es importante clasificar el tumor, es decir, determinar en qué fase se encuentra.
El sistema que con mayor frecuencia se emplea para su clasificación es el TNM. Estas siglas hacen referencia a 3 aspectos del cáncer: la T se refiere al tamaño del mismo, la N a la afectación de los ganglios linfáticos y la M a la afectación o no de otros órganos.
En función de estos aspectos, el cáncer de próstata se agrupa en las siguientes etapas o estadios.
- Estadio I: el cáncer no es palpable ni visible por medios diagnósticos. Su diagnóstico es accidental (cuando el paciente acude por otros motivos al urólogo).
- Estadio II: tumor palpable o visible que no sobrepasa la próstata. El tumor no se ha diseminado fuera de la próstata.
- Estadio III: el cáncer sobrepasa la cápsula y afecta a tejidos que rodean la próstata como las vesículas seminales.
- Estadio IV: El tumor se ha diseminado a los ganglios linfáticos o a otras partes del organismo, como los huesos.
La agresividad de las células tumorales se clasifica mediante un sistema denominado Gleason que determina distintas categorías de agresividad de las células. Este nombre corresponde a la del patólogo norteamericano que propuso los distintos grados.Sistema de Gleason
Este sistema valora el aspecto y distribución que las glándulas tumorales presentan al microscopio. Distingue varios tipos (grados o patrones de Gleason) clasificándolos en 5 categorías diferentes de menor a mayor agresividad. Éstas se expresan con números del uno al cinco, correspondiendo el 1 a los tumores menos agresivos y el 5 para los más agresivos.
Debido a que las células dentro del mismo cáncer de próstata no siempre son del mismo grado, actualmente se identifican los dos patrones más predominantes y se suman, obteniendo lo que se conoce como suma de Gleason o "score" de Gleason.
Este oscila entre 2 (1+1) el mínimo y 10 (5+5) el más agresivo. Hasta el grado 6 se consideran los tumores menos agresivos, del 8 hasta el 10 se incluyen los más agresivos y el tumor de grado 7 se considera intermedio.
Elección del tratamiento
Una vez que se ha confirmado el diagnóstico de cáncer de próstata y se han realizado las pruebas necesarias para conocer en qué fase está la enfermedad, se debe determinar cuál es el tratamiento más adecuado para curarla.
El especialista le recomendará y explicará las posibilidades de tratamiento más indicadas en su caso, para que una vez que haya recibido la suficiente información pueda, junto con su médico tomar una decisión.
El tratamiento del cáncer de próstata, como ocurre en la mayoría de los tumores, es un tratamiento multidisciplinar. Distintas especialidades trabajan juntas para combinar terapias y ofrecer al paciente las mayores posibilidades de curación.
En el tratamiento del cáncer de próstata se sigue un protocolo, es decir un conjunto de normas y pautas (plan de tratamiento) que se establecen, basándose en la experiencia científica, para el tratamiento de dicho tumor.
Estos protocolos, que se emplean de forma generalizada en todos los hospitales, recogen las indicaciones o limitaciones de tratamiento en función de una serie de factores:- Estadio de la enfermedad.
- Agresividad de las células cancerosas (suma o "score" de Gleason).
- Niveles de PSA en el momento del diagnóstico.
- Edad y esperanza de vida estadística independientemente del cáncer de próstata.
- Preferencias del paciente.
Probablemente, el médico también tendrá en cuenta si además del cáncer de próstata, existen otras enfermedades importantes, que puedan dificultar la realización de algún tratamiento específico.El tratamiento propuesto por el especialista no va a ser el mismo en todos los pacientes
Los tratamientos más frecuentemente empleados en el cáncer de próstata son la observación y vigilancia, la cirugía, la radioterapia y la hormonoterapia.
En los siguientes apartados se describen cada uno de ellos tratando de explicar en qué consisten, qué efectos adversos producen y cuáles son las recomendaciones para minimizar dichos efectos.Cáncer de próstata en estadio I
El tratamiento del cáncer de próstata en estadio I puede incluir los siguientes procedimientos:
- Espera atenta.
- Prostatectomía radical, habitualmente con linfadenectomía pélvica, con radioterapia o sin ella después de la cirugía. Puede ser posible extirpar la próstata sin dañar los nervios necesarios para la erección.
- Radioterapia de haz externo.
- Radioterapia con implante.
Cáncer de próstata en estadio II
El tratamiento del cáncer de próstata en estadio II puede incluir los siguientes procedimientos:
- Prostatectomía radical, con linfadenectomía pélvica o sin ella. Se puede administrar radioterapia después de la cirugía. Puede ser posible extirpar la próstata sin dañar los nervios necesarios para la erección.
- Espera atenta.
- Radioterapia de haz externo con terapia hormonal o sin esta.
- Radioterapia con implante.
Cáncer de próstata en estadio III
El tratamiento del cáncer de próstata en estadio III puede incluir los siguientes procedimientos:
- Radioterapia de haz externo con terapia hormonal o sin ella.
- Terapia hormonal.
- Prostatectomía radical, con linfadenectomía pélvica o sin ella. Se puede administrar radioterapia después de la cirugía.
- Espera cautelosa.
- Radioterapia, terapia hormonal o resección transuretral de la próstata como tratamiento paliativo para aliviar los síntomas causados por el cáncer.
Cáncer de próstata en estadio IV
El tratamiento del cáncer de próstata en estadio IV puede incluir los siguientes procedimientos:
- Terapia hormonal.
- Radioterapia de haz externo con terapia hormonal o sin ella.
- Radioterapia o resección transuretral de la próstata como tratamiento paliativo para aliviar los síntomas causados por el cáncer.
- Espera atenta.
Opciones de tratamiento para el cáncer de próstata recidivante
El tratamiento del cáncer de próstata recidivante puede incluir los siguientes procedimientos:
- Radioterapia.
- Prostatectomía para pacientes inicialmente tratados con radioterapia.
- Terapia hormonal.
- Medicamentos para el dolor, radioterapia externa, radioterapia interna con radioisótopos como estroncio-89, u otros tratamientos como terapia paliativa para reducir el dolor de hueso.
Cirugía
El tipo de cirugía que se puede aplicar en el cáncer de próstata, varía en función del tamaño, de la localización y de la extensión de la enfermedad a ganglios y/o órganos vecinos.
La cirugía a nivel de la próstata es una intervención quirúrgica mayor, por lo que es necesario un ingreso hospitalario durante un tiempo que puede variar de un enfermo a otro, pero por lo general suele oscilar entre una y dos semanas. Asimismo, es necesario una anestesia, que siempre será de tipo general.
Se lleva a cabo mediante una intervención denominada prostatectomía radical. Se realiza como tratamiento definitivo y su objetivo es conseguir la curación del cáncer.
Generalmente, su indicación es, exclusivamente, para aquellos pacientes con enfermedad limitada a la glándula prostática.
Consiste en la extirpación de la glándula prostática por completo. Además, se extirpan también las vesículas seminales con las que se encuentra íntimamente relacionada, y en determinadas ocasiones, se hará una extirpación de los ganglios linfáticos regionales que sirven de drenaje a la próstata.Una vez completada la extirpación, la vejiga de la orina y la uretra quedan desconectadas, ya que también se extirpa la porción de uretra que atraviesa la próstata. A continuación, el cirujano procederá a unir estas estructuras mediante puntos de sutura, colocando además una sonda urinaria que deberá llevar durante unos días.
Tras la intervención, siempre y cuando todo discurra sin complicaciones, permanecerá hospitalizado durante unos días, generalmente una semana, al cabo de los cuales será dado de alta. Lo habitual es que se vaya a su casa con la sonda urinaria y los puntos de sutura de la herida quirúrgica.
Después de una prostatectomía radical desaparecerá la emisión de semen debido a que las estructuras extirpadas son las que lo producen, prácticamente, en su totalidad.
Actualmente, las técnicas quirúrgicas para practicar una prostatectomía radical son:- PROSTATECTOMÍA RADICAL RETROPÚBICA: se llega a la próstata a través del abdomen, realizando una incisión desde el ombligo hasta el pubis. Tras la intervención quedará una cicatriz en dicha zona. Su práctica es la más extendida actualmente.
- PROSTATECTOMÍA RADICAL PERINEAL: en este caso la extirpación de la próstata se hace mediante una incisión practicada en el periné (área existente entre el ano y la bolsa escrotal que alberga los testículos).
- PROSTATECTOMÍA RADICAL LAPAROSCÓPICA: consiste en practicar varias punciones en la cavidad abdominal que permiten colocar unos tubos (trocares) a través de los cuales el cirujano opera mirando las imágenes recogidas por una cámara en un monitor de televisión. Esta técnica permite extraer la próstata y vesículas seminales sin dejar herida quirúrgica. Tan sólo quedan unas pequeñas cicatrices correspondientes a las incisiones realizadas para situar los trocares.
Quimioterapia
La quimioterapia en el cáncer de próstata avanzado se indica en pacientes que no responden o hayan dejado de responder al tratamiento hormonal.
Tratamiento hormonal
Desde hace años se sabe que el cáncer de próstata es un tumor, en la mayoría de los casos, dependiente de las hormonas y, particularmente, de los andrógenos.
Estos son producidos en su mayor parte (90-95%) en los testículos en forma de testosterona y el resto (5-10%) en las glándulas suprarrenales, que se encuentran situadas encima de ambos riñones. Los andrógenos actúan sobre la próstata estimulando la proliferación de las células tumorales.
Los tratamientos hormonales se utilizan sobre todo cuando la enfermedad está diseminada o bien como complemento de alguno de los tratamientos locales o en las recaídas que pueden presentarse tras dichos tratamientos.
La eficacia del tratamiento hormonal se basa en suprimir la testosterona de la sangre, y por tanto el efecto que esta tiene sobre el cáncer de próstata, lo que ocurre en el 80% de los casos.
La supresión de los andrógenos se va a conseguir mediante tratamiento farmacológico (medicamentos) o mediante tratamiento quirúrgico, extirpando los testículos o su tejido productor de testosterona (orquidectomía).
- Orquidectomía: generalmente se efectúa una extirpación de la parte interior del testículo donde está el tejido productor de testosterona. Es una intervención sencilla que requiere anestesia y una breve hospitalización que, generalmente, no supera 24 horas. Los efectos hormonales derivados de la orquidectomía son inmediatos produciéndose un descenso eficaz sobre el cáncer de próstata en menos de 24 horas.
Este tratamiento no es reversible y genera una deprivación de testosterona definitiva.
- Tratamiento farmacológico: consiste en obtener la supresión de la testosterona mediante medicamentos (análogos de la LHRH) que actúan sobre la hipófisis consiguiendo que los testículos dejen de producir esta hormona. Esto se logra mediante unas inyecciones que permiten que el efecto dure hasta tres meses, con la consiguiente comodidad, ya que sólo serán necesarias cuatro inyecciones al año. Para evitar la acción de los andrógenos procedentes de la glándula suprarrenal se utilizan los antiandrógenos. En ocasiones, se usan conjuntamente con los análogos de la LHRH conociéndose esta modalidad de tratamiento como bloqueo hormonal completo.
El tratamiento con medicamentos tiene la ventaja de ser reversible, de manera que si aparecen efectos secundarios, se puede suspender volviendo a una situación hormonal igual a la existente antes del tratamiento. Los inconvenientes son que tiene que preocuparse de tomar la medicación con la periodicidad prescrita por el especialista, y que tardan unas semanas en alcanzar su eficacia. Con el tiempo, el tratamiento hormonal puede fracasar al proliferar células que presentan la característica de ser resistentes a las hormonas, produciéndose entonces la progresión de la enfermedad, situación que se conoce como hormonoresistencia.
Efectos secundarios
Tras la deprivación de andrógenos en la sangre aparecen ciertos efectos secundarios que pueden disminuir la calidad de vida. Entre los más importantes destacan la aparición de impotencia, disminución de la líbido (deseo sexual), aumento de peso, desarrollo discreto de las mamas, debilidad muscular, anemia, osteoporosis y sofocos.(deseo sexual), aumento de peso, desarrollo discreto de las mamas, debilidad muscular, anemia, osteoporosis y sofocos.
¿Es necesario permanecer aislado?
En ocasiones, mientras tenga colocados los implantes es necesario que permanezca en una habitación, preparada especialmente para tal fin.
El paciente estará controlado, en todo momento, a través de un monitor de televisión por el personal sanitario responsable de su cuidado.
¿Cuánto dura el tratamiento?
La duración del tratamiento dependerá en gran medida del tipo de isótopo que se haya empleado en el implante y de la cantidad de dosis que se quiera administrar en la zona del tumor, pero generalmente oscila entre minutos y días.Radioterapia
La radioterapia es el empleo de radiaciones ionizantes para el tratamiento, local o locorregional, de determinados tumores que emplea rayos X con altas dosis de irradiación.
Las radiaciones ionizantes poseen la capacidad de destruir las células tumorales en la zona donde son aplicadas. Desde hace tiempo se conoce la sensibilidad del cáncer de próstata a determinadas radiaciones, por lo cual la radioterapia constituye un tratamiento muy eficaz para esta enfermedad.
Es un tratamiento local cuyo objetivo es, al igual que la cirugía, conseguir la curación del cáncer. Generalmente, como tratamiento exclusivo está indicado en pacientes con tumores localizados en la próstata. Cuando el tumor está localmente avanzado (tumores que sobrepasan los límites de la próstata) se consigue, en ocasiones, el control tumoral y la mejoría de la calidad de vida.
Existen dos modalidades de aplicación de la radioterapia:
- Radioterapia externa: consiste en la administración de las radiaciones desde el exterior mediante unos equipos generadores de radiación (aceleradores lineales), que no contactan con el paciente y emiten y proyectan estas sobre la próstata.
- Braquiterapia: la radiación se administra mediante fuentes de material radiactivo colocadas en estrecho contacto con la próstata.
Existen dos tipos de braquiterapia en la próstata: implantes permanentes y temporales.
El tratamiento con radioterapia siempre es individualizado, es decir, cada enfermo tendrá su tratamiento específico y distinto al de otro paciente.
Según la finalidad con que se emplee, la radioterapia puede ser curativa o paliativa para aliviar síntomas provocados por el cáncer de próstata tales como el dolor óseo.
En los últimos años los avances de la tecnología han permitido mejorar la eficacia de este tratamiento disminuyendo, notablemente, sus efectos secundarios. Con los modernos equipos de radioterapia (conformacional en tres dimensiones y de intensidad modulada) se calcula y administra al tumor la dosis de radiación con gran precisión, minimizando la dosis que reciben los tejidos sanos de alrededor de la próstata.
Planificación del tratamiento con RT:
Antes de empezar con el tratamiento propiamente dicho, es preciso realizar una planificación o simulación del mismo. Su finalidad es determinar una serie de parámetros que variarán dependiendo del tipo, de la localización y de la extensión del tumor, así como de las características anatómicas de cada enfermo.
Durante todo el tratamiento, el paciente ha de permanecer inmóvil y mantener la misma postura. Es frecuente, que próximo a la zona del tumor se encuentren determinadas estructuras importantes como la vejiga, el recto, las cabezas femorales, el bulbo peneano, entre otros. Para administrar la radiación con una precisión elevada y evitar que los tejidos sanos que rodean al tumor reciban más dosis de la tolerada, se utilizan sistemas de inmovilización muy precisos para que permitan la administración de la radiación con gran exactitud.
Habitualmente, para realizar el cálculo de la dosis que va a recibir tanto el tumor como los tejidos sanos de alrededor del mismo, es necesario realizar una tomografía de localización, cuyas imágenes se introducen en la computadora, donde se determina el volumen de tratamiento.
Antes de la realización de la tomografía se determina el sistema de inmovilización más adecuado para cada paciente según la técnica que se vaya a aplicar.
Una vez realizada la planificación, estos sistemas de fijación permiten su reproducción diaria en la sala de tratamiento.
¿Dónde se realiza el tratamiento con radioterapia?
Las habitaciones donde se realizan los tratamientos de radioterapia externa se llaman salas de radioterapia o búnkeres. Estas habitaciones poseen paredes de hormigón con un gran espesor que proporcionan un aislamiento perfecto impidiendo que la radiación salga fuera de ellas.
Mientras dura la sesión de tratamiento el paciente estará solo en el interior de la sala, pero vigilado por el personal especializado a través de un circuito de televisión y un interfono.
¿Por qué es necesario acudir todos los días?
Si se administrara toda la dosis de radiación en una única sesión se producirían daños muy serios en los tejidos. Para minimizar estos efectos secundarios, la dosis total de radiación se fracciona, repartiéndose en un número determinado de sesiones y días.
El fraccionamiento estándar consiste en administrar una sesión al día durante cinco días a la semana descansando dos, generalmente sábados y domingos. Para su administración no es necesario estar ingresado, puede acudir al hospital para el tratamiento y una vez finalizado volver a su casa.¿Cuánto dura el tratamiento?
El tratamiento de radioterapia suele durar entre dos y siete semanas, dependiendo de la dosis que se administre y del número total de sesiones.
Diariamente, cada sesión dura sólo unos minutos (quince aproximadamente). El tiempo real de irradiación dura unos segundos.
Una vez finalizado el tratamiento diario, puede estar en contacto con otras personas, ya que no emite ningún tipo de radiactividad. Sus relaciones sociales, laborales y familiares no tienen por qué verse afectadas mientras dure el tratamiento.
Efectos secundarios:
La radioterapia, al mismo tiempo que elimina células enfermas, puede afectar a los tejidos sanos cercanos al área de tratamiento y como consecuencia aparecen efectos secundarios en la zona que ha recibido el tratamiento.
Estos efectos son difíciles de prever con exactitud, ya que dependen de múltiples factores como la zona del organismo donde se realiza el tratamiento, la dosis, el fraccionamiento y la susceptibilidad individual de cada persona. En algunos casos se producen efectos mínimos, mientras que en otros son más serios y es necesario administrar tratamiento médico para su control..
Radioterapia interna
Es una técnica de tratamiento que consiste en introducir en el interior del organismo isótopos radiactivos. Se pueden implantar de forma temporal o permanente en la zona a tratar.
Con la radioterapia interna se logra administrar altas dosis de radiación a cortas distancias, de tal forma, que llega muy poca dosis a los tejidos sanos circundantes al implante.
¿Cómo se colocan los implantes?
Dependiendo del tipo de implante que se vaya a realizar es necesario permanecer ingresado en el hospital durante 1 o dos días, en otros casos el paciente podrá irse a su casa el mismo día tras recibir el tratamiento. Bajo sedación o anestesia general, se efectuará la colocación de los isótopos radiactivos.Incontinensia Urinaria
La pérdida involuntaria de la orina puede aparecer tras el tratamiento. Se produce como consecuencia de la proximidad de la próstata al esfínter urinario, el cual durante el procedimiento terapéutico puede verse lesionado, así como algunas de las estructuras involucradas en la continencia.
Esta situación produce un insuficiente funcionamiento de los mecanismos responsables en la retención urinaria y, por consiguiente, la aparición de incontinencia. La edad es un factor de riesgo, de modo que los enfermos de más edad son los que con mayor frecuencia presentan incontinencia postoperatoria.
La pérdida de orina puede ser diferente según los casos, distinguiéndose tres tipos:
- Urgencia miccional: en esta circunstancia la vejiga se contrae sin haber voluntad de hacerlo, provocando un intenso deseo de orinar que obliga a la micción.
- Incontinencia de esfuerzo: los escapes de orina ocurren cuando se realizan movimientos o ejercicios que aumentan la presión en el abdomen como puede ser al moverse súbitamente, correr, levantarse de una silla, etc.
- Incontinencia total: es la pérdida constante y continua de orina no llegando a realizar micciones, o pocas, debido a que no se llega a almacenar prácticamente orina en la vejiga.
Las primeras medidas que se pueden adoptar para mejorar esta situación son la restricción de líquidos y realización de ejercicios que están destinados a fortalecer los músculos del suelo de la pelvis, ayudando a disminuir la incontinencia.
Si las pérdidas son cuantiosas y ha transcurrido el tiempo suficiente como para considerar que es una incontinencia establecida, se pueden plantear tratamientos para mejorar o resolver esta.
Tratamiento de la incontinencia
Este tratamiento consiste en intervenciones quirúrgicas que llevan a cabo la inyección de substancias como colágena o silicona a través de la uretra en las proximidades del esfínter, produciendo el cierre parcial de éste.
Otra solución más compleja, es la colocación de un esfínter artificial mediante un manguito alrededor de la uretra, que al llenarse de líquido cierra la uretra.
Dispositivos para la incontinencia urinaria
La incontinencia puede variar en su intensidad requiriendo desde el uso de una pequeña gasa de protección, pasando por el empleo de compresas hasta llegar a la necesidad de tener que llevar pañal, con la consiguiente incomodidad y afectación psicológica y social.
Actualmente, existen en el mercado una importante variedad de dispositivos adaptados a las distintas necesidades de cada paciente que permiten, de forma discreta y eficaz, paliar las incomodidades y alteraciones de la pérdida de orina proporcionando la posibilidad de seguir llevando una vida normal.
- Absorbente masculino: su uso está indicado, principalmente, en aquellos pacientes con incontinencia de goteo. Se trata de una compresa fina y absorbente en forma de bolsa con una gran capacidad de absorción. Este material asegura la retención de toda la humedad sin posibilidad de fuga.
- Cooreslect: Se trata de un sistema fabricado con un material sintético sin látex e hipoalergénico, que se adapta al pene como un preservativo, quedando sujeto a él por una tira autoadhesiva, que evita que se mueva y exista pérdida de orina.
Existen varias modalidades y tamaños para adaptarse a las distintas necesidades de los pacientes.
El colector drena hacia una bolsa de recogida de orina, que mediante unas cintas se fija a la pierna (como si se tratara de un liguero). Es un sistema cómodo y discreto que permite desarrollar la actividad diaria normalmente.Disfunción sexual
Es la alteración en la capacidad de erección o de su duración, impidiendo o dificultando la actividad sexual. Es una circunstancia que ocurre con cierta frecuencia tras los tratamientos del cáncer de próstata.
En los primeros momentos después de conocer el diagnóstico, este aspecto puede pasar a un segundo plano dando prioridad a la curación de la enfermedad. Después del tratamiento, con el paso del tiempo llega a ser una preocupación importante que produce un grado de insatisfacción considerable que altera la calidad de vida. Esto se hace más evidente cuanto más joven es el paciente.
Es muy frecuente que tras los tratamientos se produzca una falta de emisión de semen con el orgasmo, esta situación se conoce como orgasmo seco. La satisfacción de la actividad sexual no tiene por qué verse afectada.
La disfunción sexual se produce como consecuencia de la lesión o extirpación de los nervios y vasos sanguíneos responsables de la erección en el tratamiento quirúrgico o la radioterapia. Si no se preservan, la práctica totalidad permanecen impotentes. Hay que tener presente que la preservación de los nervios de la erección no se puede hacer en todos los pacientes sometidos a prostatectomía radical.
Influyen claramente, la edad y la función sexual previa al tratamiento. Cuanto mayor es la edad en el momento del tratamiento mayores probabilidades hay de perder la función sexual después del mismo. En el caso de tener la potencia sexual alterada antes de la cirugía o radioterapia, esta se va a ver afectada con mayor frecuencia.
En el caso de la cirugía, la pérdida de la función sexual prácticamente es inmediata recuperándose lentamente incluso hasta dos años después de la misma. La frecuencia con la que esta capacidad de erección se mantiene o recupera varía con la técnica empleada (entre un 40 y 60% cuando se preservan indemnes los nervios), siendo mayor este porcentaje cuanto menor es la edad del enfermo.
En el caso de la radioterapia, la pérdida de la potencia sexual se produce poco a poco después del tratamiento, a medida que las radiaciones hacen su efecto sobre los tejidos.
Existen diversos tratamientos mediante los cuales se puede mejorar la potencia sexual consiguiendo una erección que permita desarrollar una actividad sexual para el enfermo y su pareja.
- Tratamiento farmacológico: mediante la utilización de medicamentos en forma de pastillas que facilitan las respuestas naturales al estímulo sexual a nivel del pene. Estos tratamientos no son eficaces en todos los enfermos sometidos a tratamiento por cáncer de próstata pero, en muchos de ellos, ayudan a mejorar este aspecto recuperando la calidad de vida alterada por esta circunstancia.
- Dispositivos de vacío: son unos mecanismos mediante los cuales se consigue el relleno del pene con la sangre por succión, alcanzando una turgencia considerable del mismo. Esta se mantiene con la colocación de un anillo constrictor en la base del pene.
Tratamiento quirúrgico: son las prótesis de pene. Existen diversos modelos en el mercado con las cuales se consigue una erección implantando unos cilindros en el interior del pene, que permiten obtener una turgencia adecuada para poder mantener una actividad sexual satisfactoria. La colocación requiere una operación que puede presentar complicaciones por la propia intervención o por el fallo en el funcionamiento de alguno de los mecanismos de la prótesis.- Pulmon (Cáncer)
Cáncer que se forma en los tejidos del pulmón, por lo general, en las células que recubren las vías respiratorias. Los dos tipos más importantes de cáncer de pulmón son el cáncer de pulmón de células pequeñas y el cáncer de pulmón de células no pequeñas. Estos tipos de cáncer se diagnostican con base en el aspecto que tengan las células bajo un microscopio.
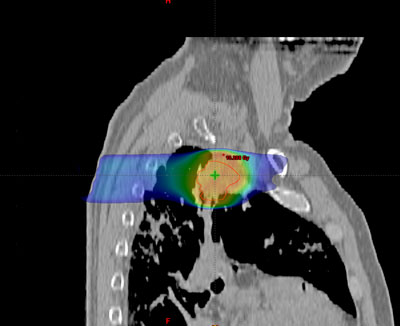
Los distintos tipos histológicos tienen diferente evolución natural y, por tanto, como paso previo al tratamiento, es necesario un diagnóstico histológico preciso realizado por un anatomopatólogo experto. Las principales decisiones con respecto al tratamiento se toman al distinguir claramente un carcinoma de célula pequeña y los que no corresponden a este tipo (subclasificados a su vez en diferentes tipos histológicos).
Las formas más comunes de cáncer de pulmón reciben nombres que dependen de las características de las células de las cuales derivan, distinguiéndose dos grandes grupos:
Carcinomas de células pequeñas o microcítico: su nombre deriva del tamaño de sus células (microcítico: células muy pequeñas). Un 20% de los cánceres de pulmón son de este tipo. Se localiza preferentemente en la zona central de los pulmones, pudiendo comprimir a vasos u órganos localizados en ese nivel (vena cava, etc.). Se caracterizan por su alta agresividad y crecimiento rápido.
Carcinomas no microcíticos: representan el 80% restante de los cánceres de pulmón. Los tipos más frecuentes son:
- Carcinoma escamoso o epidermoide: es la variedad de cáncer broncopulmonar más frecuente en nuestro país, representando el 40% de los carcinomas no microciticos. Suele localizarse en la parte central de los pulmones, y con frecuencia se necrosa en su interior y se asemeja a un absceso. Tiene un crecimiento relativamente lento.
- Adenocarcinoma: representa el 30% de los carcinomas no microcíticos. Es el menos relacionado con el consumo de tabaco, pero aún así es más frecuente en fumadores. Suele aparecer más entre las mujeres y localizarse en zonas más periféricas de los pulmones, por lo que frecuentemente afectan a la pleura y pared torácica. En los últimos años, esta variante histológica ha cobrado especial interés al descubrirse que un subgrupo de pacientes tienen una alteración molecular (mutación del EGFR) que permite ser tratados con fármacos de diana terapéutica.
Carcinoma de células grandes: se denomina así por el tamaño de las células que lo componen. Es el tipo menos frecuente de los carcinomas broncopulmonares, representando el 10% de ellos.
- Para poder emitir un juicio sobre el pronóstico del enfermo y determinar el tratamiento más adecuado, es importante clasificar el tumor, es decir, determinar en qué fase se encuentra.
El sistema que con mayor frecuencia se emplea para su clasificación es el TNM. Estas siglas hacen referencia a tres aspectos del cáncer: la T se refiere al tamaño y localización del tumor, la N a la afectación de los ganglios linfáticos y la M a la afectación o no de otros órganos.Tumor primario (T):
- T0 - No hay signos de un tumor primario.
- TX - Cáncer oculto, demostrado en la citología del lavado bronquial pero no radiológicamente ni en la fibrobroncoscopia. Las secreciones broncopulmonares contienen células malignas pero no hay otros datos de la existencia de un cáncer de pulmón.
- TIS - Carcinoma in situ.
- T1 - Tumor menor o igual de 3 cm de dimensión máxima, rodeado por tejido pulmonar o pleural visceral y sin invasión proximal al bronquio lobar en la fibrobroncoscopia.
- T2 - Tumor mayor de 3 centímetros de dimensión mayor o tumor de cualquier tamaño que invade la pleura visceral o con atelectasia (colapso del pulmón) o neumonitis obstructiva que se extiende a la región hiliar. En la broncoscopia, la extensión proximal del tumor puede limitarse al bronquio lobar o estar al menos a 2 cm de la carina. La atelectasia o la neumonitis obstructiva no deben afectar a todo un pulmón.
- T3 - Tumor de cualquier tamaño con extensión directa a la pared costal (incluidos los tumores de la cisura superior) diafragma, pleura mediastínica o pericardio, sin afectación del corazón, grandes vasos, tráquea, esófago, cuerpos vertebrales o un tumor del bronquio principal a menos de 2 cm de la carina, sin infiltración de la misma. La atelectasia afecta a todo un pulmón. Existe derrame pleural no maligno.
- T4 - Tumor de cualquier tamaño con infiltración del mediastino o del corazón, grandes vasos, tráquea, esófago, cuerpos vertebrales o carina o con derrame pleural maligno. Los derrames pleurales no hemáticos ni exudativos y con varios estudios citológicos negativos no se clasifican como malignos con fines de determinación del estadio.
Ganglios linfáticos regionales (N):- N0 - Sin metástasis demostrables en los ganglios linfáticos
- N1 - Metástasis en los ganglios linfáticos peribronquiales o hiliares ipsolaterales, o ambos, incluyendo la extensión directa del tumor.
- N2 - Metástasis en los ganglios mediastínicos o subcarinales ipsilaterales.
- N3 - Metástasis en los ganglios mediastínicos o hiliares contralaterales, escaleno ipso o contralateral o supraclaviculares.
Metástasis a distancia (M):- M0 - Sin metástasis a distancia conocidas.
- M1 - Metástasis a distancia presentes, especificando su localización por ejemplo en cerebro.
Elección del tratamiento
Una vez que se ha confirmado el diagnóstico de cáncer de pulmón, y se han realizado las pruebas necesarias para conocer en qué fase está la enfermedad, se debe determinar cuál es el tratamiento más adecuado para curarla. El especialista recomendará y explicará las posibilidades de tratamiento más óptimas en cada caso, para que el paciente con toda la información pueda junto con el médico tomar una decisión.
El tratamiento del cáncer de pulmón, como ocurre en la mayoría de los tumores, es multidisciplinar. Distintas especialidades trabajan juntas para combinar terapias y ofrecer al paciente las mayores posibilidades de curación. Fundamentalmente colaboran neumólogos, radiólogos, anatomopatólogos, cirujanos y oncólogos.
En el tratamiento del cáncer de pulmón se sigue un protocolo, es decir un conjunto de normas y pautas (plan de tratamiento), establecidas en base a la experiencia científica que se tiene en el tratamiento de este tumor.
Estos protocolos, que se emplean de forma generalizada en todos los hospitales, recogen las indicaciones o limitaciones del tratamiento en función de los siguientes factores:
- Fase o estadio en la que se encuentra la enfermedad (TNM).
- Tipo de tumor: carcinomas microcíticos y no microcíticos.
Características del paciente: edad, enfermedades que dificulten algún tratamiento específico, estado nutricional…
- El tratamiento propuesto por el especialista no va a ser el mismo en todos los pacientes.
Los tratamientos más frecuentemente empleados en el cáncer de pulmón son la cirugía, la radioterapia y la quimioterapia. Además el médico se encargará de tratar específicamente los síntomas que presenta cada enfermo.Cáncer de pulmón de células pequeñas
Cáncer de pulmón de células pequeñas en estadio limitado
El tratamiento del cáncer de pulmón de células pequeñas en estadio limitado puede incluir los siguientes procedimientos:- Quimioterapia de combinación y radioterapia dirigida al pecho. Más tarde, se puede administrar radioterapia dirigida al cerebro para pacientes con respuestas completas.
- Quimioterapia de combinación para pacientes con problemas pulmonares que están muy enfermos. Más tarde, se puede administrar radioterapia dirigida al cerebro para pacientes con respuestas completas.
- Cirugía, seguida por quimioterapia o quimioterapia más radioterapia dirigida al pecho. Más tarde, se puede administrar radioterapia dirigida al cerebro para pacientes con respuestas completas.
Cáncer de pulmón de células pequeñas en estadio extensivo
El tratamiento del cáncer de pulmón de células pequeñas en estadio extensivo puede incluir los siguientes procedimientos:
- Quimioterapia de combinación. Más tarde, se puede administrar radioterapia dirigida al cerebro para pacientes con respuestas completas.
- Radioterapia dirigida al cerebro, la médula, los huesos u otras partes del cuerpo en las cuales se ha diseminado el cáncer, como terapia paliativa para aliviar los síntomas y mejorar la calidad de vida.
Opciones de tratamiento para el cáncer de pulmón de células pequeñas recidivante
El tratamiento del cáncer recidivante de pulmón de células pequeñas puede incluir los siguientes procedimientos:
- Quimioterapia.
- Radioterapia, como terapia paliativa para aliviar los síntomas y mejorar la calidad de vida.
- Terapia láser, colocación de una derivación para mantener abiertas las vías respiratorias o radioterapia interna como tratamiento paliativo para aliviar los síntomas y mejorar la calidad de vida.
Cáncer de pulmón de células no pequeñas
Cáncer de pulmón de células no pequeñas oculto
El tratamiento del cáncer de pulmón de células no pequeñas oculto depende del sitio hasta donde el cáncer se diseminó. Por lo general, se puede curar mediante cirugía.
Estadio 0 (carcinoma in situ)
El tratamiento del estadio 0 puede incluir los siguientes procedimientos:
- Cirugía (resección en cuña o resección segmentaria).
- Terapia fotodinámica con el uso de un endoscopio.
- Electrocauterización, criocirugía o cirugía láser con el uso de un endoscopio.
Cáncer de pulmón de células no pequeñas en estadio I
El tratamiento del cáncer de pulmón de células no pequeñas en estadio I puede incluir los siguientes procedimientos:
- Cirugía (resección en cuña, resección segmentaria, resección en manguito o lobectomía).
- Radioterapia externa (para pacientes que no pueden o eligen no someterse a cirugía).
Cáncer de pulmón de células no pequeñas en estadio II
El tratamiento del cáncer de pulmón de células no pequeñas en estadio II puede incluir los siguientes procedimientos:
- Cirugía (resección en cuña, resección segmentaria, resección en manguito o lobectomía, o neumonectomía).
- Radioterapia externa (para pacientes que no pueden o eligen no someterse a cirugía).
- Cirugía seguida de quimioterapia.
Cáncer de pulmón de células no pequeñas en estadio IIIA
El tratamiento del cáncer de pulmón de células no pequeñas en estadio IIIA que se puede extirpar por medio de cirugía puede incluir los siguientes procedimientos:
- Cirugía seguida de quimioterapia.
El tratamiento del cáncer de pulmón de células no pequeñas en estadio IIIA
que no se puede extirpar por medio de cirugía puede incluir los siguientes procedimientos:
- Quimioterapia combinada con radioterapia.
- Radioterapia externa sola (para pacientes que no se pueden tratar con terapia combinada).
El cáncer de pulmón de células no pequeñas del surco superior, que a menudo se llama tumor de Pancoast, empieza en la parte superior del pulmón y se disemina hasta los tejidos cercanos como las costillas y las vértebras. El tratamiento de los tumores de Pancoast puede incluir los siguientes procedimientos:
- Radioterapia sola.
- Radioterapia y cirugía.
- Cirugía sola.
- Quimioterapia combinada con radioterapia y cirugía.
Algunos tumores de pulmón de células no pequeñas en estadio IIIA que crecieron en la pared torácica se pueden extirpar completamente. El tratamiento de los tumores de la pared torácica puede incluir los siguientes procedimientos:
- Cirugía.
- Cirugía y radioterapia.
- Radioterapia sola.
- Quimioterapia combinada con radioterapia o cirugía.
Cáncer de pulmón de células no pequeñas en estadio IIIB
El tratamiento del cáncer de pulmón de células no pequeñas en estadio IIIB puede incluir los siguientes procedimientos:
- Quimioterapia combinada con radioterapia externa.
- Radioterapia externa como terapia paliativa para aliviar el dolor y otros síntomas, y mejorar la calidad de vida.
Cáncer de pulmón de células no pequeñas en estadio IV
El tratamiento del cáncer de pulmón de células no pequeñas en estadio IV puede incluir los siguientes procedimientos:
- Radioterapia externa, como terapia paliativa para aliviar el dolor y otros síntomas, y mejorar la calidad de vida.
- Quimioterapia de combinación.
- Quimioterapia de combinación y terapia dirigida.
- Terapia láser o radioterapia interna con el uso de un endoscopio.
Opciones de tratamiento para el cáncer de pulmón de células no pequeñas recidivante
El tratamiento del cáncer de pulmón de células no pequeñas recidivante puede incluir los siguientes procedimientos:
- Radioterapia externa, como terapia paliativa para aliviar el dolor y otros síntomas, y mejorar la calidad de vida.
- Quimioterapia o terapia dirigida.
- Cirugía (para algunos pacientes que tienen una cantidad muy baja de cáncer que se diseminó hasta el cerebro).
- Terapia láser o radioterapia interna con el uso de un endoscopio.
- Radiocirugía (para ciertos pacientes que no pueden someterse a cirugía).
Cirugía
La cirugía es la primera opción de tratamiento, la más eficaz, en los cánceres no microcíticos en estadios localizados. En los carcinomas microcíticos, la primera opción de tratamiento es la quimioterapia.
El tipo de cirugía dependerá del tamaño, localización y extensión del tumor. Cuando se extirpa un lóbulo pulmonar (cada una de las partes en las que está dividido el pulmón) se llama lobectomía, cuando lo que se extirpa es todo un pulmón hablamos de neumonectomía.
La cirugía a nivel del pulmón es una intervención mayor, por lo que es necesario un ingreso hospitalario que puede variar de un enfermo a otro, pero que por lo general suele oscilar entre una y dos semanas.Asimismo, precisa anestesia, que siempre será de tipo general.
Para llevar a cabo la intervención se debe realizar una toracotomía, es decir una incisión en el tórax, que permita al cirujano llegar hasta la zona tumoral. Si solamente está afectado un lóbulo se hace una lobectomía.
Si están afectados más de un lóbulo o el bronquio principal, la intervención necesaria es la neumonectomía. Normalmente se extirpan los ganglios mediastínicos para ver si están o no afectados por el tumor.Quimioterapia
Tratamiento adyuvante (tras la cirugía)
Los pacientes con carcinoma de pulmón no microcítico sometidos a una resección completa, presentan, sin embargo, un elevado riesgo de recidiva (50% en el estadio IB, 70% en el II y un porcentaje todavía mayor de los pacientes con tumores en estadio IIIB). Es por ello que el uso de quimioterapia adyuvante (tras la cirugía) se ha estudiado desde hace varias décadas. Los primeros estudios, que se realizaron en los años 70 y 80 del siglo XX, identificaron a los derivados del platino como agentes activos para el tratamiento de este tipo de cáncer.
En los últimos años se han realizado varios ensayos clínicos para explorar la efectividad y forma de administración óptima de los regímenes de poliquimioterapia (basados en combinaciones con sales de platino). Los estudios más importantes publicados recientemente (IALT, BIG, ALPI, ANITA y JBR10), exploraban diferentes combinaciones de cisplatino (principalmente con vinorelbina) y encontraron un beneficio en cuanto supervivencia global y supervivencia libre de progresión.
Es por ello que se ofrece la posibilidad de recibir quimioterapia adyuvante en aquellos pacientes operados de cáncer de pulmón en estadio II ó III.
Tratamiento de la enfermedad localmente avanzada
El tratamiento del carcinoma no microcítico de pulmón localmente avanzado es un campo de investigación activa en el momento actual.
Generalmente, los pacientes en estadio IIIA según la clasificación de estadificación anatomopatológica suelen ser sometidos a cirugía y posteriormente tratados con quimioterapia adyuvante.
A los pacientes con derrame tumoral pleural o pericárdico suele ofrecérseles quimioterapia paliativa ya que, a pesar de que actualmente se clasifica estos casos como IIIB, el pronóstico y la evolución de estos pacientes es similar al de aquellos con enfermedad extratorácica.
De hecho, en la revisión propuesta de la clasificación TNM, estos tumores se consideran estadio IV.
Para el resto de pacientes con tumores en estadio III, el tratamiento varía entre la administración de quimio y radioterapia neoadyuvantes, seguida de resección quirúrgica y un número variable de ciclos de quimioterapia de consolidación, ó la utilización de quimiorradioterapia concomitante (esto es, darlos conjuntamente).
Tratamiento de la enfermedad avanzada
El valor del tratamiento quimioterápico para los pacientes con carcinoma no microcítico de pulmón metastásico se puso de manifiesto a raíz de los estudios en los que se comparaba el tratamiento con quimioterapia basada en cisplatino y tratamiento de soporte frente al tratamiento de soporte sin quimioterapia.
Se observó una diferencia estadísticamente significativa en supervivencia global a favor del tratamiento quimioterápico.
Existen múltiples agentes activos en el tratamiento del CPNCP, que se han utilizado tanto en combinación como en monoterapia.
Los más utilizados son los derivados de platico (cisplatino y carboplatino), los taxanos (paclitaxel y docetaxel), vinorelbina, gemcitabina, etopósido y permetrexed.
En los últimos años se han producido avances muy significativos en el tratamiento del cáncer de pulmón, incorporando nuevos fármacos dirigidos a dianas específicas de las células tumorales. Es el caso de los fármacos dirigidos al EGFR ( receptor del factor de crecimiento epidérmico) o al VEGF (factor de crecimiento derivado del endotelio vascular)Otros tratamientos
Láser intrabronquial
Cuando el desarrollo del tumor es intrabronquial, es decir dentro del conducto del bronquio, puede obstaculizar el paso del aire dificultando gravemente la respiración.En estos casos puede tratarse la lesión con láser, para destruir parte del tumor, permitir el paso del aire, y disminuir así el ahogo del paciente. El láser se aplica con la ayuda de un endoscopio introducido en las vías respiratorias.
Prótesis endobronquiales
Esta técnica, como la anterior, se utiliza cuando el desarrollo del tumor ocupa el interior de los bronquios impidiendo el paso del aire.Consiste en colocar mediante endoscopia una especie de tubo más o menos rígido a la altura de la zona del bronquio obstruida por el tumor, con el objetivo de facilitar la respiración del paciente.
Radiofrecuencia
En los últimos años han aparecido técnicas de ablación con catéteres de lesiones únicas pulmonares en pacientes inoperables.Esta técnica consiste en quemar la lesión mediante un catéter que se introduce en el pulmón. Suele usarse en tumores menores de 4 cm y todavía no es una técnica estándar de tratamiento.
Radioterapia
La radioterapia es el empleo de radiaciones ionizantes para el tratamiento, local o locorregional, de determinados tumores que emplea rayos X con altas dosis de irradiación.
Su objetivo es destruir las células tumorales causando el menor daño posible a los tejidos sanos que rodean dicho tumor. El tipo de radioterapia utilizada en el cáncer de pulmón es la externa. Para ello se emplean máquinas de gran tamaño (aceleradores lineales), que en ningún momento contactan con el enfermo.
La radioterapia puede emplearse como tratamiento único o en combinación. Se puede administrar antes de la intervención para disminuir su tamaño y facilitar la cirugía o después de la misma, para limpiar la zona de la cirugía de las posibles células tumorales que hayan podido quedar. Asimismo, se puede administrar con la quimioterapia para potenciar sus efectos (quimioirradiación).
El tratamiento con radioterapia siempre es individualizado, es decir, cada enfermo tendrá su tratamiento específico y distinto al de otro paciente.
En el cáncer de pulmón la utilización de la radioterapia varía en función del tipo de cáncer:
- En los cánceres de pulmón no microcíticos, la radioterapia se utiliza cuando es imposible realizar la cirugía por el riesgo que supone para el paciente, el tumor es inoperable o como tratamiento de algunas metástasis. Puede combinarse con quimioterapia.
- En los carcinomas microcíticos, la radioterapia se utiliza como tratamiento complementario a la quimioterapia en los casos en que la enfermedad está localizada. También está indicada en la prevención y tratamiento de metástasis cerebrales.
Según la finalidad con que se emplee, la radioterapia puede ser curativa o paliativa para aliviar síntomas provocados por el cáncer de pulmón o las metástasis. Este es el caso de la radioterapia antiálgica, utilizada en las lesiones óseas con el objetivo de disminuir el dolor que producen al paciente.
Planificación del tratamiento con RT:
Antes de empezar con el tratamiento propiamente dicho, es preciso realizar una planificación o simulación del mismo. Su finalidad es determinar una serie de parámetros que variarán dependiendo del tipo, de la localización y de la extensión del tumor, así como de las características anatómicas de cada enfermo.
Durante todo el tratamiento, el paciente ha de permanecer inmóvil y mantener la misma postura. Es frecuente, que próximo a la zona del tumor se encuentren determinadas estructuras importantes como el corazón, la medula espinal, las cabezas humerales, el hígado, el estomago, entre otros. Para administrar la radiación con una precisión elevada y evitar que los tejidos sanos que rodean al tumor reciban más dosis de la tolerada, se utilizan sistemas de inmovilización muy precisos para que permitan la administración de la radiación con gran exactitud.
Habitualmente, para realizar el cálculo de la dosis que va a recibir tanto el tumor como los tejidos sanos de alrededor del mismo, es necesario realizar una tomografía de localización, cuyas imágenes se introducen en la computadora, donde se determina el volumen de tratamiento.
Antes de la realización de la tomografía se determina el sistema de inmovilización más adecuado para cada paciente según la técnica que se vaya a aplicar.
Una vez realizada la planificación, estos sistemas de fijación permiten su reproducción diaria en la sala de tratamiento.
¿Dónde se realiza el tratamiento con radioterapia?
Las habitaciones donde se realizan los tratamientos de radioterapia externa se llaman salas de radioterapia o búnkeres. Estas habitaciones poseen paredes de hormigón con un gran espesor que proporcionan un aislamiento perfecto impidiendo que la radiación salga fuera de ellas.
Mientras dura la sesión de tratamiento el paciente estará solo en el interior de la sala, pero vigilado por el personal especializado a través de un circuito de televisión y un interfono.
¿Por qué es necesario acudir todos los días?
Si se administrara toda la dosis de radiación en una única sesión se producirían daños muy serios en los tejidos. Para minimizar estos efectos secundarios, la dosis total de radiación se fracciona, repartiéndose en un número determinado de sesiones y días.
El fraccionamiento estándar consiste en administrar una sesión al día durante cinco días a la semana descansando dos, generalmente sábados y domingos. Para su administración no es necesario estar ingresado, puede acudir al hospital para el tratamiento y una vez finalizado volver a su casa.
¿Cuánto dura el tratamiento?
El tratamiento de radioterapia suele durar entre dos y siete semanas, dependiendo de la dosis que se administre y del número total de sesiones.
Diariamente, cada sesión dura sólo unos minutos (quince aproximadamente). El tiempo real de irradiación dura unos segundos.
Una vez finalizado el tratamiento diario, puede estar en contacto con otras personas, ya que no emite ningún tipo de radiactividad. Sus relaciones sociales, laborales y familiares no tienen por qué verse afectadas mientras dure el tratamiento.
Efectos secundarios:
La radioterapia, al mismo tiempo que elimina células enfermas, puede afectar a los tejidos sanos cercanos al área de tratamiento y como consecuencia aparecen efectos secundarios en la zona que ha recibido el tratamiento.
Estos efectos son difíciles de prever con exactitud, ya que dependen de múltiples factores como la zona del organismo donde se realiza el tratamiento, la dosis, el fraccionamiento y la susceptibilidad individual de cada persona. En algunos casos se producen efectos mínimos, mientras que en otros son más serios y es necesario administrar tratamiento médico para su control..
Radioterapia internaEs una técnica de tratamiento que consiste en introducir en el interior del organismo isótopos radiactivos. Se pueden implantar de forma temporal o permanente en la zona a tratar.
Con la radioterapia interna se logra administrar altas dosis de radiación a cortas distancias, de tal forma, que llega muy poca dosis a los tejidos sanos circundantes al implante.
¿Cómo se colocan los implantes? Dependiendo del tipo de implante que se vaya a realizar es necesario permanecer ingresado en el hospital durante 1 o dos días, en otros casos el paciente podrá irse a su casa el mismo día tras recibir el tratamiento. Bajo sedación o anestesia general, se efectuará la colocación de los isótopos radiactivos.
¿Es necesario permanecer aislado? En ocasiones, mientras tenga colocados los implantes es necesario que permanezca en una habitación, preparada especialmente para tal fin.
El paciente estará controlado, en todo momento, a través de un monitor de televisión por el personal sanitario responsable de su cuidado.
¿Cuánto dura el tratamiento? La duración del tratamiento dependerá en gran medida del tipo de isótopo que se haya empleado en el implante y de la cantidad de dosis que se quiera administrar en la zona del tumor, pero generalmente oscila entre minutos y días.
.png)
